viernes, 26 de noviembre de 2021
EL VIRUS DEL NILO
¿SE PUEDE ELIMINAR EL VIH SIN TRATAMIENTO ALGUNO?
Una mujer argentina de 31 años a la que se le encontró la presencia de VIH en 2013 y que únicamente había recibido terapia antirretroviral durante 6 meses de embarazo para no transmitir la infección al bebé. Tras múltiples pruebas en busca de evidencias genéticas del VIH en la sangre volvieron a no encontrar ni rastro del virus. Se trataría del segundo caso de paciente curada.
Los médicos creen que el sistema inmune de la paciente eliminó por si solo el virus causante del síndrome de inmunodeficiencia adquirida (SIDA). Los científicos creen que si logran descubrir como se produjo el proceso podrían encontrar un via para encontrar una cura definitiva para el VIH. El hallazgo supone una prueba más de que algunas personas nacen con una resiliencia natural frente al virus, algunos tienen genes que previenen la infección y otros parecen haber sido capaces de eliminar el virus después de haberlo contraido.Sin embargo en los últimos años algunos informes han mostrado la existencia de los llamandos controladores de élite, que pueden suprimir el virus con ayuda, pero sin medicación.
Xu Yu, miembro del Instituto Ragon, del Hospital general de Massachusetts en Estados Unidos, estudia como el VIH almacena copias de su genoma en las células humanas, creando lo que se conoce como un reservorio viral. En este estado el virus el virus se esconde eficazmente de los medicamentos contra el VIH y de la respuesta inmunitaria del organismo. En la mayoría de las personas se producen constantemente nuevas particulas virales a partir de este reservorio.
La terapia antirretroviral (TAR) puede impedir que se produzcan nuevos virus, pero no puede eliminar el reservorio, por lo que es necesario un tratamiento diario para suprimir el virus. Sin embargo, las personas conocidas como controladores de élite tienen sistemas inmunitarios capaces de suprimir el VIH sin necesidad de medicación. Aunque siguen teniendo reservorios virales que pueden producir más virus del VIH, un tipo de célula inmunitaria células T asesinas parecen mantener al virus inoperativo sin necesidad de medicación.
En la mayoria de las personas que conviven con el VIH éstas células cumplen su función, auque de una manera ineficiente, lo que explica que la infección persista. En los casos de la paciente Argentina y Loreen Willenberg sus células T fueron muy eficientes y podrían haber eliminado todas las células que contenían virus enteros.
Vídeo: VIH y SIDA
Fuente(s): BBC, National Geographic, El Mundo
LA DIVISIÓN DEL NÚCLEO SE CONTROLA DESDE FUERA
La meiosis es la división celular encargada de la formación de los gametos, es decir, de los óvulos y los espermatozoides necesarios para la reproducción. Mediante este proceso, las células que contienen los 46 cromosomas que posee el ser humano, reducen su número a la mitad formando los gametos, que solo tienen un único conjunto de 23 cromosomas, un par en los espermatozoides y otro par en los óvulos.
Los errores que se producen durante este proceso derivan en gametos defectuosos que pueden ser la causa de abortos espontáneos, enfermedades genéticas e infertilidad. “Por eso las células meióticas poseen mecanismos de vigilancia o checkpoints que aseguran que los gametos reciben el número adecuado de cromosomas. Estos mecanismos son como alarmas, que son necesarias para estar seguros de que, en caso de una emergencia, se responda adecuadamente para evitar peligrosas consecuencias”, explica Beatriz Santos, científica del IBFG y coautora del proyecto.Para que el mecanismo de control actúe de forma adecuada, la presencia de la proteína Pch2 en los distintos compartimentos celulares como nucléolo, citoplasma y cromosomas, debe ser equilibrada. "Conocer cómo funcionan estas alarmas celulares podría ayudar a entender mejor las posibles alteraciones que subyacen a las patologías reproductivas y, a largo plazo, contribuir a su prevención", concluye San-Segundo.
Fuentes: Info Salus, Nova Ciencia
LAS ESPONJAS MARINAS, LA RESPUESTA AL ORIGEN DEL SISTEMA NERVIOSO
El 4 de noviembre de 2021, se ha publicado en la revista ‘Science’ un estudio que anuncia sobre un sistema de comunicación celular que aplican las esponjas para regular la alimentación y eliminar microbios.
Las neuronas de los animales se comunican mediante reacciones químicas a través de la sinapsis. Los científicos han descubierto que las esponjas marinas tienen ciertos genes que codifican proteínas las cuales participan de ayudantes en la sinapsis, lo más sorprendente es la inexistencia de neuronas en estas.
Detlev Arendt y un grupo de científicos del Laboratorio Europeo de Biología Molecular en Heidelberg, secuenciaron ARN proveniente de células de la Spongilla lacustris, una esponja de agua dulce.
Los investigadores han descubierto que la esponja marina contiene 18 diferentes tipos de células. Los genes sinápticos que se situaban en los alrededores de las cámaras digestivas de las esponjas de mar, estaban activos, con esto los científicos encargados de la investigación sugirieron que la forma de comunicación celular podía compaginar la alimentación por filtración. Los escáneres utilizados por estos profesionales para estudiar las células, las cuales llamaron Neuroides Secretoras, mostraron que, para alcanzar los coanocitos, envían unas extensas ramas.
Los científicos piensan que las extensas ramas anteriormente mencionadas posibilitan la comunicación con los coanocitos, así deteniendo el sistema de agua eliminando residuos y microbios sin identificar. Pero las Neuroides Secretoras no son nervios, con lo cual no hay signos de sinapsis que conceden a las neuronas comunicarse velozmente. Sin embargo, estas células podrían haberse adherido al sistema nervioso de los animales, concretamente a la sinapsis, durante el proceso de la evolución. El origen del sistema nervioso podría encontrarse en las esponjas marinas.
ACTIVIDAD ELÉCTRICA DEL CORAZÓN
Un estudio internacional dirigido por la Universidad Complutense de Madrid ha dado un paso más para comprender mejor cómo funcionan los mecanismos que controlan la actividad eléctrica del corazón.
Los científicos han descubierto una función desconocida de la proteína Tbx20 que regula la actividad eléctrica de las células cardíacas en el corazón adulto.
Hasta ahora se pensaba que el papel de la proteína Tbx20 se limitaba al período embrionario, cuando regulaba la formación del corazón.
Una investigación internacional dirigida por profesores de la Universidad Complutense de Madrid (UCM) ha descubierto que esta proteína también regula la actividad eléctrica de las células cardíacas en el corazón adulto.
Para llegar a esta conclusión, los investigadores identificaron los genes responsables del síndrome de QT Largo (SQTL) en dos generaciones de una familia española. “Esta enfermedad hereditaria puede aparecer como consecuencia de mutaciones en al menos quince genes”, explica Eva Delpón, investigadora del departamento de Farmacología de la UCM y del Centro de Investigación Biomédica en Red (CIBER), y autora principal del estudio publicado en la revista PNAS.
Los pacientes afectados por esta enfermedad presentan alteraciones en la actividad eléctrica de su corazón, lo que favorece la aparición de arritmias que pueden desencadenar la muerte de forma súbita.
“En muchos casos, las arritmias o la muerte asociadas a este síndrome se producen en niños, incluso lactantes, o jóvenes aparentemente sanos, por lo que la muerte a veces es el primer y último síntoma de la enfermedad”, señala Delpón. En el caso de la familia estudiada, en una generación de seis hermanos dos chicas murieron antes de cumplir los 20 años.
“Hemos identificado un nuevo gen (TBX20) cuyas mutaciones pueden ser responsables de la aparición de un nuevo tipo de síndrome de QT Largo”, afirma la científica. Aunque el hallazgo no va a variar el tratamiento de estos pacientes, el estudio ayuda a comprender mejor la complejidad de los mecanismos que controlan la actividad eléctrica del corazón.
Además, según los autores, se identifica así una nueva diana cuya modulación podría tener interés terapéutico en un futuro. El estudio clínico se ha llevado a cabo en el Servicio de Cardiología del Hospital Universitario La Paz (Madrid), dirigido por José Luis López-Sendón, que también participa en el trabajo.
Los científicos han identificado una mutación en el gen TBX20 que codifica el factor de transcripción Tbx20. Los resultados han demostrado que dicho factor regula, a su vez, la expresión del gen KCNH2, que codifica la expresión de una proteína (Kv11.1). Esta proteína forma unas estructuras (canales iónicos) en las células cardíacas que permiten el paso de iones potasio.
Los miembros de la familia que tienen la mutación en Tbx20 tienen menos canales de potasio en las células musculares de su corazón, lo que altera sus propiedades eléctricas, produciendo el síndrome y las arritmias.
Los expertos confirmaron estos resultados en células cardíacas humanas (cardiomiocitos) diferenciadas a partir de células madre pluripotentes inducidas (IPSc, que poseen la capacidad de generar células de distintos tipos de tejidos). Estas células, a su vez, se obtuvieron a partir de fibroblastos de la piel de individuos sanos.
“Nosotros no disponíamos de estos cardiomiocitos derivados de IPSc, por lo que un miembro de nuestro equipo, Ricardo
Caballero, se desplazó al laboratorio de Jose Jalife en la Universidad de Ann Arbor (EEUU) para realizar los experimentos”, destaca Delpón.
El estudio ha sido posible gracias a la colaboración del grupo de investigación de la UCM con los servicios de cardiología de seis hospitales públicos de la Comunidad de Madrid en el marco del consorcio ITACA. Este consorcio está dirigido por Juan Tamargo, profesor de la facultad de Medicina de la UCM, y está financiado gracias a un Proyecto de Investigación Biomédica concedido por la Comunidad de Madrid.
Fuente: Agencia SINC
EXPERIMENTO CON EMBRIONES QUE CONTIENEN CÉLULAS DE MONO Y HUMANO
Los embriones de mono con células humanas son ya una realidad de laboratorio.
Una investigación llevada a cabo por investigadores en EE.UU. y China lo ha logrado, generando un nuevo debate sobre la ética de este tipo de experimentos.
Los científicos inyectaron células madre humanas -aquellas que pueden desarrollarse en tejidos corporales diferentes- en embriones de macacos.
Los embriones en cuestión fueron estudiados por un máximo de 20 días.
Otros embriones de especies mixtas, o quimeras (en referencia a los monstruos con cabeza de león, vientre de cabra y cola de dragón de la mitología griega), han sido desarrollados en el pasado, implantando células humanas en embriones de oveja o cerdo.
El equipo de científicos en cuestión estuvo liderado por el profesor Juan Carlos Izpisúa Belmonte del Instituto Salk de EE.UU., que ya ayudó en 2017 a crear el primer híbrido humano-cerdo.
Su trabajo podría abrir el camino para solucionar la grave escasez de órganos para trasplantes, así como ayudar a entender más el desarrollo humano temprano, la progresión de las enfermedades y el envejecimiento, señaló el profesor.
"Estos enfoques quiméricos podrían ser realmente útiles para avanzar en la investigación biomédica, no solo en la etapa más temprana de la vida, sino también en la última".
El profesor mantiene que el estudio, publicado en la revista especializada Cell, cumplió con las directrices éticas y legales actuales.
"En última instancia, efectuamos estos estudios para entender y mejorar la salud humana", subrayó.
Sin embargo, algunos científicos han manifestado su preocupación por el experimento, argumentando que pese a que los embriones en este caso fueron destruidos a los 20 días, otros podrían tratar de llevar el trabajo un paso más allá. Estos piden un debate público sobre las implicaciones de crear quimeras de especies mixtas (humanas-no humanas).
En referencia a la investigación, Anna Smajdor, investigadora de ética biomédica de la Escuela de Medicina de Norwich, de la Universidad de East Anglia, en Inglaterra, considera que ésta presenta "desafíos legales y éticos significativos".
"Los científicos detrás de esta investigación señalan que estos embriones quimera ofrecen nuevas oportunidades, porque 'no somos capaces de llevar a cabo ciertos tipos de experimentos en humanos'. Pero si esos embriones son humanos o no es una cuestión no resuelta".
El profesor Julian Savulescu, director del Centro Uehiro para la Ética Práctica de la Universidad de Oxford, y codirector del Centro Wellcome de Éticas y Humanidades, consideró que el estudio "abre la caja de Pandora a quimeras humanas-no humanas".
"Estos embriones fueron destruidos a los 20 días de desarrollo, pero es solo cuestión de tiempo que las quimeras humanas-no humanas sean desarrolladas con éxito, quizá como fuente de órganos para humanos", añadió.
"Ese es uno de los objetivos a largo plazo de esta investigación".
Sarah Norcross, directora del británico Progress Educational Trust, considera que, pese a que se han realizado "avances sustanciales" en la investigación de embriones y células madre, que podrían aportar beneficios sustanciales, "hay una clara necesidad de discusión y debate público sobre los desafíos éticos y regulatorios que genera".
Fuente: BBC
jueves, 25 de noviembre de 2021
¿SON TODOS LOS PRIONES MALOS?
Todos tenemos priones. Estos son proteínas de estructura anómala que actúan como agentes infecciosos ocasionando enfermedades neurodegenerativas transmisibles, llamadas encefalopatías espongiformes, como la enfermedad de Creutzfeldt-Jakob o el kuru en humanos; la enfermedad de las vacas locas o la tembladera o scrapie en cabras y ovejas.
¿Por qué se han ganado esta mala fama? En los priones se presentan dos configuraciones, una útil, normal, y otra infecciosa, mal plegada y nociva. En este caso, aunque la proteína no llegue a la estructura deseada, no se destruye, ambas configuraciones son tridimensionales estables. La configuración nociva resulta inmune a los sistemas de limpieza del organismo, por lo que se acumulan y atacan al cerebro. Además, cuando un prion mal plegado llega al cerebro, los de alrededor cambian su configuración, teniendo unos resultados que acaban siendo mortales.
Pero, los priones también tienen una función útil en las células que aíslan los nervios. Estos priones ayudan a mantener la vaina de mielina en las células que protegen los nervios, abundando en las propias neuronas. Y, controlan la dirección de la plasticidad en el hipocampo en desarrollo, estructura cerebral relacionada, entre otras cualidades, con la memoria y el aprendizaje, informa el Journal of Neuroscience.
SE CREAN LAS PRIMERAS CÉLULAS ARTIFICIALES PARA COMBATIR A LOS VIRUS
¿ESTAMOS MÁS CERCA DE CLONAR HUMANOS?
Los detalles del experimento de Shanghái permiten albergar dudas sobre su verdadero propósito, aparte de mostrar que China se ha situado en la primera división científica. Desde que en 1997 el equipo de Ian Wilmunt, del Instituto Roslin de Edimburgo, presentó el primer mamífero obtenido por clonación, la famosa ovejita Dolly, se han clonado ya 26 especies de mamíferos por la misma técnica: la transferencia nuclear. Consiste en obtener el ADN de una célula adulta del animal que se quiere clonar e introducirlo en un ovocito de una hembra donante al que previamente se ha extraído su núcleo. Ello da lugar a un embrión cuyo material genético es idéntico al del animal clonado.
El equipo asegura que la finalidad del experimento es obtener primates para la experimentación médica, pero sus propios colegas del Instituto Roslin lo ponen en cuestión. Consideran que hay otras vías más eficaces y seguras de conseguir animales de experimentación, por ejemplo utilizando la nueva técnica de edición genética CRISPR.
La cuestión es: si en un momento determinado se demostrara una forma viable y segura de clonar primates a partir de células adultas, ¿cuánto tiempo se mantendría la barrera que prohíbe intentarlo en humanos? En los años setenta se produjo un debate similar respecto de la fecundación in vitro. En ese momento se planteaban muchas objeciones éticas y también científicas, pues muchos investigadores estaban convencidos de que la técnica produciría anomalías en los fetos y por ello desaconsejaban intentarlo siquiera. En medio de la polémica, dos científicos, Robert Edwards y Patrick Steptoe, decidieron echarse a la piscina. Y hoy hay millones de niños que fueron concebidos en la probeta. En España, el 20% de los que nacen.
UN ANIMAL MULTICELULAR QUE SOBREVIVIÓ COGELADO 24.000 AÑOS
Este proceso de criogenización, que consiste en conservar a los seres vivos por largos periodos de tiempo a bajas temperaturas, es el mismo que ha permitido que este animal multicelular conocido como rotífero bdeloideo haya sobrevivido congelado durante más de 24.000 años, según reveló un estudio publicado recientemente en la revista científica Current Biology.
Una vez descongelado, este organismo microscópico pudo reproducirse en un proceso llamado partenogénesis, en el que las células sexuales femeninas no son fecundadas por el macho, sino que el óvulo se segmenta por sí mismo y logra desarrollarse en un nuevo ser sin que haya sido fertilizado por un espermatozoide.
"Nuestro informe es la prueba más convincente de que a día de hoy los animales multicelulares podrían soportar decenas de miles de años en criptobiosis, el estado en el que el metabolismo se detiene casi completamente", afirma Malavin. Y añade: "En el futuro podríamos preservar organismos con sus órganos intactos casi para siempre, pero para eso necesitamos estudiar cómo lo hace la naturaleza".
El Laboratorio de Criología del Suelo que encontró este rotífero multicelular lleva más de tres décadas aislando organismos microscópicos de las capas más frías y remotas de Siberia. Durante el proceso han identificado muchos microbios unicelulares, un gusano nematodo de miles de años de antigüedad y musgos y plantas que también se han regenerado después de decenas de miles de años congelados en el hielo.Fuentes: El país
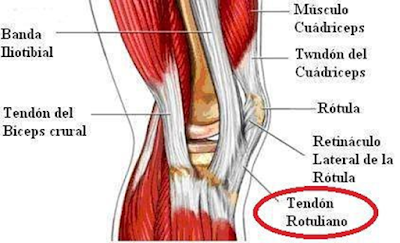
REGENERAR TENDONES YA ES POSIBLE
NUEVAS CELULAS ANTI-VIRUS
El estudio dirigido por MRC, en Cambridge, Inglaterra, su investigación puede conducir al desarrollo de nuevos polímeros (macromoléculas compuestas por muchas unidades repetidas, como proteínas, plásticos y muchos medicamentos, incluidos los antibióticos) y promover el uso de bacterias para fabricar medicamentos de manera segura.
LA INESTABILIDAD DE LOS CENTRIOLOS DERIVA A ENFERMEDADES


“Todas estas enfermedades no solo están vinculadas a defectos en la generación de microtúbulos, sino también en la estabilidad de los centriolos. Esperamos que esta nueva perspectiva nos lleve a una comprensión más profunda de estas enfermedades”, explica el Dr. Lüders. El estudio se titula “Sub-centrosomal mapping identifies augmin-γTuRC as part of a centriole-stabilizing scaffold”. Y se ha publicado en la revista académica Nature Communications.
miércoles, 24 de noviembre de 2021
VACUNA PARA BEBÉS
El estreptococo B, una bacteria que las embarazadas pueden transmitir a sus bebés, al año suele causar unas 150.000 muertes de recién nacidos al año, una cifra que podría bajar si se impulsara la investigación de vacunas tras 30 años de estancamiento, advierte hoy la Organización Mundial de la Salud.
Un nuevo informe que por primera vez muestra el impacto global de esta bacteria, elaborado por la OMS junto a la Escuela de Higiene y Medicina Tropical de Londres (LSHTM), recuerda que esto causa medio millón de partos prematuros anuales.
Además, podría provocar en niños discapacidades a largo plazo tales como parálisis cerebral, pérdida visual o auditiva.
A la luz de las elevadas cifras, la OMS "tiene prisas " por la comunidad científica para que desarrolle vacunas maternales contra este tipo de bacteria para reducir su mortalidad.
"El estreptococo tipo B es una grave amenaza, hasta ahora poco conocida, a la supervivencia y el bienestar de los recién nacidos, con devastadores efectos para muchas familias de todo el mundo", afirmó el jefe médico del departamento de Inmunización y Vacunas de la OMS, Phillipp Lambach.
Varias investigaciones de vacunas contra esta bacteria ya se han iniciado, pero según la OMS no han conseguido lanzar fármacos al mercado después de décadas de estudio.
Estimaciones del informe indican que si se lograra desarrollar una vacuna e inmunizar con ella a un 70% de las madres embarazadas podrían evitarse al menos 50.000 muertes de recién nacidos y 170.000 partos prematuros.
"La vacunación maternal podría salvar las vidas de cientos de miles de personas en los próximos años, pero se propuso hace 30 años y el mundo todavía no ha producido ninguna vacuna", comentó el profesor Joy Lawn, del LSHTM.
Como media, un 15% de las embarazadas en todo el mundo, o unos 20 millones de mujeres, son portadoras de esta bacteria, en general sin sufrir síntomas por ello, pero pueden transmitirla durante el embarazo o el parto. Las regiones con mayor número de casos de estreptococo B entre niños y niñas son aquellas con un bajo desarrollo de los cuidados pre y post-parto.
LOS VIRUS QUE NOS ACECHAN DURANTE LA COVID-19

Como puedes apreciar en la imagen de la derecha, el rinovirus, el VRS y el coxsackie son los otros virus que nos acechaban mientras nosotros solo mirábamos a la Covid-19.
Estos son los responsables de catarros y resfriados, sin embargo, la razón por la que ha costado detectarlos es la semejanza a la Covid en cuanto a síntomas y transmisión se refiere.
El rinovirus (RV) fue aislado por primera vez en 1956 por Pelon y colaboradores. Es asociado al resfriado común, del cual se dice es la infección más frecuente en humanos. Pertenece a la familia Picornaviridae a la cual pertenece también la polio, los enterovirus y el virus hepatitis A.El coxsackie es un virus que afecta a las manos, pies y boca provocando erupciones con ampollas, se transmite a través del contacto de las secreciones de mucosa y saliva. Provoca además fiebre, inapetencia, rinorrea y dolor de garganta.
El virus respiratorio sincitial (VRS) provoca una bronquiolitis. El VRS es un virus respiratorio que suele causar síntomas leves y parecidos al resfriado común. Su riesgo es sobre todo para bebés, mayores o enfermos crónicos a los que puede causar infecciones pulmonares graves al igual que la Covid.El argentino Pablo Murcia, virólogo en la Universidad de Glasgow (Escocia), explica en una entrevista con EFE los hallazgos de un estudio sobre el coronavirus difundido este martes que revela, entre otras cosas, que “el virus del resfriado común puede ofrecer protección transitoria contra el covid”. Su investigación con células en el laboratorio, publicada en la revista estadounidense “Journal of Infectious Diseases”, demuestra que una infección con rinovirus responsable del resfriado genera “una respuesta innata” en el ser humano que parece bloquear la progresión del SARS-CoV-2. Esto significa, por una parte, que cuando una persona tiene el virus del resfriado, quedaría protegida del covid, aunque solo durante unos días.
LAS CÉLULAS DE LA GLÍA Y SU POTENCIAL TERAPÉUTICO TRAS UNA ISQUEMIA CEREBRAL
La isquemia es una patología neurodegenerativa que está provocada por el bloqueo del flujo sanguíneo cerebral o su disminución. Esta enfermedad es la primera causa de discapacidad permanente y la segunda de mortalidad a nivel mundial. En la actualidad, sólo hay un único tratamiento que ha sido aprobado, la reperfusión. Esto es solo posible durante las primeras horas después del ictus, lo que deja un número reducido de pacientes aptos para esta intervención, además de no evitar la pérdida de funciones cerebrales a largo plazo.
BIORREMEDIACIÓN CON BACTERIAS ANIQUILADORAS DE PETRÓLEO
Murphy, que se sentía profundamente preocupado por el desastroso vertido de petróleo de la plataforma Deepwater Horizon en el Golfo de México hace diez años, centró su investigación en ello para así ayudar a informar sobre futuras estrategias de mitigación de vertidos de petróleo.
En la investigación, simularon la neutralización de derrames de petróleo dentro de botellas, combinando el lodo de los primeros centímetros del lecho marino del Ártico con agua de mar artificial y gasóleo o petróleo crudo, junto con diferentes enmiendas nutritivas a distintas concentraciones.
Estas simulaciones demostraron que las bacterias que degradan el petróleo de forma natural en el océano son las primeras en responder a un vertido de petróleo.
Nuevos sistemas de secuenciación genómica han permitido revelar que Bacterias como la Paraperlucidibaca, la Cycloclasticus, la Oleispira, la Thalassolituus o la Zhongshania, que viven en el mar del Labrador entre Canadá y Groenlandia, son capaces de metabolizar el petróleo. De este modo, limpian el océano, asegurando que siga siendo un recurso vital para las comunidades de los alrededores.
 Este proceso biotecnológico consistente en aprovechar las capacidades catabólicas de seres vivos, en su mayoría microorganismos, hongos o plantas para recuperar un medio ambiente alterado por contaminantes a su condición natural, recibe el nombre de biorremediación.
Este proceso biotecnológico consistente en aprovechar las capacidades catabólicas de seres vivos, en su mayoría microorganismos, hongos o plantas para recuperar un medio ambiente alterado por contaminantes a su condición natural, recibe el nombre de biorremediación.Por ello, la biotecnología que controla y manipula deliberadamente sistemas biológicos, principalmente células o componentes celulares, con el objeto de generar o procesar productos y materias primas, es una de las pocas alternativas que podemos emplear si queremos proteger el medio ambiente, reducir el uso de pesticidas y fertilizantes químicos, a la vez que conseguir plantas más productivas y resistentes que alimenten a la creciente población humana.
martes, 23 de noviembre de 2021
NUEVAS TERAPIAS GÉNICAS BASADAS EN UN SISTEMA UTILIZADO POR VIRUS

Ya que los genes artificiales pueden producir efectos dañinos o incluso peligrosos cuando se manifiestan en las células erróneas, los científicos quisieron descubrir un modo de minimizar estos efectos perjudiciales de las terapias génicas. Una forma de diferenciar los distintos tipos de células son las secuencias de ARN de su interior, ya que son diferentes según el tejido.
Al descubrir una manera de producir transgenes después de leer secuencias de ARN dentro de las células, los investigadores desarrollaron una tecnología para poder perfeccionar las terapias génicas. Así, los investigadores podrían crear terapias nuevas para destruir tumores diseñando un sistema para reconocer las células cancerosas y fabricar una proteína tóxica dentro de esas células, matándolas en el procedimiento.

Años atrás, se desarrolló un modo de usar la detección de ARN como disparador para activar a las células a producir una proteína específica en las bacterias. Este método funciona mediante la introducción de una molécula de ARN, llamada puntera, que se une al ribosoma de una molécula de ARNm que codifica una proteína determinada. Esta unión evita la traducción del ARNm, ya que no puede juntarse con el ribosoma.
La punta de ARN también incluye una secuencia que consigue unirse a otra secuencia de ARNm que vale de activador. Si se localiza esta secuencia de ARNm objetivo, el asidero suelta su agarre y el ARNm que había sido bloqueado se traduce en proteína. Este ARNm puede codificar cualquier gen, como una molécula reportera fosforescente. Esa señal fluorescente muestra a los investigadores una forma de ver si se ha detectado la secuencia de ARNm objetivo.
En el estudio actual, los científicos se propusieron diseñar un procedimiento parecido pero que pudiera utilizarse en células eucariotas. Debido a que en
ellas es más difícil la traducción de los genes, los componentes genéticos que se usaron en las bacterias no podían introducirse en las células humanas. En vez de eso, los investigadores aprovecharon un sistema que utilizaban los virus mediante el cual conseguían que células eucariotas tradujeran sus propios genes virales, es decir, utilizaban a las células eucariotas para que hicieran un trabajo que ellos no podían hacer. Este sistema se basa en unas moléculas de ARN llamadas sitios de entrada al ribosoma interno (IRES), que pueden reclutar ribosomas y empezar la traducción del ARN.
Los científicos comenzaron con IRES naturales de distintos tipos de virus y los transformaron para poder añadir una secuencia que se una a un ARNm desencadenante. Cuando el IRES modificado se añade en una célula humana delante de un gen artificial de salida, se impide la traducción de ese gen a no ser que se detecte el ARNm desencadenante en el interior de la célula. El desencadenante hace que el IRES se recupere y deje que el gen se traduzca formando una proteína.
Se demostró que se podían reconocer las células cancerosas a través de la ingeniería de punteros que localizan el ARNm de la tirosinasa, una enzima que elabora demasiada melanina en las células de melanoma. A partir de esto, los investigadores podrían desarrollar terapias que originen la fabricación de una proteína que provoque la muerte de la célula cuando se reconozcan proteínas cancerígenas.
Todos los estudios necesarios para realizar esta investigación se realizaron en células cultivadas en una placa de laboratorio.
Fuentes: El Acarigueño, Im Médico Hospitalario, Invdes
domingo, 21 de noviembre de 2021
¿POSITIVO EN COVID CON VACUNAS PUESTAS?
"Con la aparición de nuevas variantes con potencial para evadir la inmunidad, cobra especial importancia el poder medir el número de personas vacunadas que se infectan", explica la investigadora del ISGlobal Carlota Dobaño, primera autora del estudio.
Desde el inicio de la pandemia, Dobaño y su equipo han seguido la producción y duración de anticuerpos contra diferentes antígenos virales en dos cohortes de personal sanitario en Cataluña (SeroCov y CoviCatCentral).
En este estudio, realizado en colaboración con el Instituto Catalán de la Salut (ICS), describen un descubrimiento: las vacunas a base de ARNm (Pfizer-BioNTech o Moderna) inducen la producción de anticuerpos que no solo reconocen la proteína Spike, sino que también pueden reconocer una región de la proteína N (la región C terminal) del SARS-CoV-2.
El equipo investigador observó que, tras la vacunación, había un aumento significativo de anticuerpos IgG capaces de reconocer el fragmento C terminal de la proteína N en un porcentaje considerable de casos: en el 36% de personas que recibieron la vacuna de Moderna y el 13% de aquellas a las que se administró Pfizer.
La vacuna de Moderna también indujo un aumento en anticuerpos capaces de reconocer la proteína N entera, aunque en un menor porcentaje de personas.
Este fenómeno se observó tanto en vacunados e infectados previamente por covid como en los que nunca se contagiaron, no se debe a una reactivación de la inmunidad adquirida por la infección.
De esta manera, la hipótesis más probable, según los investigadores, es que la vacunación con Spike puede inducir anticuerpos con reactividad cruzada hacia el fragmento C terminal de la proteína N.
Estos resultados son relevantes en cuanto a salud pública, ya que, como se ha propuesto usar la proteína N en los test para detectar infecciones en personas vacunadas, esto podía resultar en que "un porcentaje considerable de casos se clasificarían falsamente como infecciones asintomáticas".
Los autores concluyen así que la proteína N (o en todo caso, el fragmento C terminal) no es una buena candidata para detectar fallos vacunales y que lo mejor es usar una combinación de múltiples antígenos virales, lo que permitirá una mejor evaluación de la efectividad de las vacunas.
Fuente: El Mundo
LA NUEVA VARIANTE DEL CORONAVIRUS
Los Centros de Control de Enfermedades (CDC) de Estados Unidos ha detectado una nueva variante de la covid-19 en los procesos reglamentario...

-
Actualmente, los rinocerontes blancos ( Ceratotherium simum ) están en una situación extremadamente delicada, solo quedan 2 en Ol Pejeta Con...
-
En el mar, cada año entran entre 5 y 13 millones de toneladas de plástico y miles de especies marinas tragan fibras de este material mientra...
-
En el ámbito humano la curiosidad es parte de la vida de las personas, es difícil encontrar a alguien que no sea curioso, pero no todas las ...