jueves, 30 de noviembre de 2023
UNA VACUNA DE ARN VENCE AL CÁNCER DE PÁNCREAS
El cáncer de páncreas, conocido por ser uno de los más mortales, ha sido un desafío insuperable durante décadas, con tasas de supervivencia extremadamente bajas. Este nuevo enfoque, inspirado en la investigación de pacientes que han desafiado las expectativas de supervivencia, presenta un potencial revolucionario que podría cambiar radicalmente el panorama de tratamiento de esta enfermedad devastadora.
El ensayo clínico, que incluyó a 16 pacientes diagnosticados con adenocarcinoma ductal pancreático, demostró que la vacuna personalizada de ARN, administrada en combinación con quimioterapia e inmunoterapia, generó respuestas inmunitarias significativas en el 50% de los participantes. Más aún, ninguno de los pacientes que mostraron esta respuesta inmunitaria experimentó recaídas durante el período de seguimiento de 18 meses.
Esta vacuna, diseñada de manera específica para cada paciente según las características únicas de su tumor, se basa en la innovadora tecnología de ARN mensajero, la misma utilizada en las exitosas vacunas contra la COVID-19. El objetivo de esta aproximación personalizada es activar el sistema inmunológico, especialmente los linfocitos T asesinos, para identificar y eliminar de manera selectiva las células cancerosas.
El Dr. Balachandran y su equipo, cuyos resultados han sido publicados en la prestigiosa revista Nature, destacan que, aunque estos hallazgos son preliminares, representan un paso gigantesco y sientan las bases para la próxima fase de ensayos clínicos más extensos, con un número significativamente mayor de pacientes. Se espera que esta vacuna no solo complemente, sino que transforme los tratamientos convencionales, ofreciendo períodos de supervivencia más prolongados y potencialmente cambiando el paradigma en la lucha contra el cáncer de páncreas.
Expertos externos, como el Dr. Manel Juan del Hospital Clínic de Barcelona, elogian el estudio por su diseño sólido y destacan que estos resultados respaldan la idea de que las vacunas personalizadas de ARN son eficaces en la inducción de respuestas inmunitarias, incluso en tumores considerados poco reactivos a la inmunoterapia.
Este avance representa un hito histórico en la investigación oncológica y proporciona un rayo de esperanza para los pacientes con cáncer de páncreas, ofreciendo una perspectiva emocionante hacia tratamientos más efectivos y una potencial mejora en las tasas de supervivencia para una enfermedad que ha desafiado la ciencia durante demasiado tiempo.
Fuentes: El País, 20 Minutos
AVANCE REVOLUCIONARIO: CULTIVO DE TEJIDO CARDÍACO EN HOJAS DE ESPINACA
Aunque los científicos ya han logrado generar tejidos humanos a gran escala en laboratorios mediante métodos como la impresión 3D, cultivar vasos sanguíneos pequeños y delicados, esenciales para la salud de los tejidos, ha sido históricamente más complicado. Según informa el National Geographic, Joshua Gershlak, coautor del estudio y estudiante graduado en el Instituto Politécnico de Worcester (WPI), destaca que "la falta de una red vascular es el principal obstáculo para la ingeniería de tejidos, ya que sin ella, se produce una considerable mortalidad en los tejidos".
Una característica clave de una hoja es su enrevesada red de venas delgadas que suministran agua y nutrientes a las células. Recientemente, científicos han empleado las venas de plantas para imitar el flujo sanguíneo en el tejido humano. El procedimiento implica la modificación de una hoja de espinaca en el laboratorio, eliminando sus células vegetales y dejando un armazón de celulosa.
El propósito fundamental es reemplazar los tejidos dañados en individuos que han experimentado ataques cardíacos u otros problemas cardíacos que afectan la contracción del corazón. Así como los vasos sanguíneos, las venas en las hojas modificadas suministran oxígeno a toda la extensión del tejido de reemplazo, siendo vital en la formación de nueva materia cardíaca.
Los responsables del estudio afirman que estos mismos enfoques podrían aplicarse con diversas plantas para restaurar distintos tipos de tejidos en el cuerpo. Aunque reconocen que queda mucho trabajo por realizar, hasta ahora, los resultados son altamente prometedores.
miércoles, 29 de noviembre de 2023
LOS PELIGROS DE LAS BACTERIAS MULTIRRESISTENTES

NANOPARTÍCULAS PARA TRATAR TRASTORNOS DE LA SANGRE
Una estrategia innovadora basada en nanopartículas lipídicas cargadas con ARN mensajero ha permitido la edición del genoma de las células madre hematopoyéticas in vivo, es decir, dentro del propio organismo. Esta aproximación ha sido probada en células y modelos animales, y tiene el potencial de mejorar el tratamiento de ciertas enfermedades y favorecer el desarrollo de terapias génicas más económicas.
Las células madre hematopoyéticas son esenciales para el organismo, ya que dan origen a los diferentes tipos de células sanguíneas. Debido a su importante papel, también son herramientas terapéuticas de gran interés para tratar diversas enfermedades, como ciertos tipos de cáncer o trastornos genéticos como la anemia falciforme.
En algunos casos, las terapias con células madre hematopoyéticas se basan en la infusión de células sanas compatibles con el paciente para restaurar la funcionalidad de la médula ósea. Sin embargo, en otros casos, se requiere la modificación del ADN de las células madre para corregir la mutación responsable de la enfermedad. Hasta ahora, esta modificación solo se podía realizar fuera del organismo, en células cultivadas, lo que implicaba un proceso complejo.
Un equipo de investigadores del Hospital de Niños de Filadelfia y la Universidad de Pensilvania ha desarrollado un método para reprogramar las células madre hematopoyéticas in vivo. Utilizando nanopartículas lipídicas cargadas con ARN mensajero, lograron introducir las instrucciones genéticas necesarias para la edición genética directamente en las células madre en la médula ósea. Los resultados preliminares son prometedores y muestran un aumento significativo en la eficacia de la edición genética en células de pacientes con anemia falciforme.
Este avance tiene un potencial terapéutico importante para el tratamiento de diversas enfermedades. La modificación directa del genoma de las células madre hematopoyéticas podría ofrecer soluciones clínicas a enfermedades como la anemia falciforme y ciertos tipos de cáncer. Sin embargo, es necesario realizar más experimentos preclínicos antes de probar esta aproximación en pacientes.
Además de mejorar la eficacia y la accesibilidad de las terapias génicas con células madre hematopoyéticas, esta estrategia basada en nanopartículas lipídicas cargadas con ARN mensajero también presenta ventajas en términos de seguridad. Al dirigirse específicamente a las células madre en la médula ósea, se minimiza el riesgo de efectos secundarios no deseados en otros tejidos. Esta técnica prometedora abre nuevas posibilidades para el tratamiento de enfermedades genéticas y representa un avance significativo en el campo de la medicina regenerativa.
GENES SALTARINES ¿QUE SON? ¿QUE RELACION TIENEN CON EL ENVEJECIMIENTO?


RESUCITAN PROTEÍNAS PARA COMBATIR ENFERMEDADES ACTUALES COMO EL ALBINISMO
Los investigadores se han centrado en recrear enzimas Cas9, las moléculas que funcionan como tijeras capaces de cortar el ADN de cualquier ser vivo en un punto concreto y que son la base del sistema CRISPR de edición genética.
El CRISPR es el sistema inmune de muchas bacterias y arqueas. Les permite incrustar en su propio genoma secuencias genéticas de virus para conservar su retrato robot. Si el virus reaparece, CRISPR lo identifica y Cas9 lo mata cortando su genoma.
Expertos en edición genética de España usaron una técnica que reconstruye el genoma de organismos extintos. La técnica se conoce como reconstrucción de secuencias ancestrales. Usa potentes ordenadores para comparar los genomas completos de seres vivos actuales, cada uno compuesto por miles de millones de letras de ADN. Los investigadores han hecho un alucinante viaje en el tiempo para recuperar proteínas Cas presentes en microbios extintos. Las más antiguas que han logrado son de hace 2.600 millones de años.
La proteína más antigua de todas solo puede cortar cadenas de ADN simple, tal vez más sencillas y primitivas, el ADN humano está formado por cadena doble. Pero el resto de moléculas Cas, más recientes, sí pueden ya cortar el ADN humano con efectividad creciente y de hecho han sido capaces de corregir dos genes, TYR y OCA2, que provocan albinismo.
A principios de los años 90, el biólogo Francis Mojica dio nombre a CRISPR como parte de sus estudios de microbios que vivían en el hostil entorno de las salinas de Santa Pola (Alicante). El investigador también analizó otras secuencias llamadas PAM que son fundamentales, pues permiten al microbio distinguir entre el genoma de un virus y el suyo propio. Sin los PAM, una bacteria podría matarse a sí misma. Lo que muestra el estudio es que las Cas más antiguas cortaban sin necesidad de PAM.
Raúl Pérez-Jiménez, investigador del centro vasco de investigación cooperativa en nanociencia NanoGUNE, detalla que el hecho de que las proteínas primitivas fueran más generalistas puede ser una ventaja, pues les permite hacer cosas de las que no son capaces los CRISPR actuales, como cortar a la vez cadenas de ADN dobles y simples y también secuencias de ARN.
Miguel Ángel Moreno Pelayo, jefe de genética del Hospital Ramón y Cajal de Madrid, resalta que la reconstrucción de proteínas antiguas abre la posibilidad de diseñar nuevas formas de CRISPR sintéticas “que no existen en la naturaleza”. Entre otros proyectos, su equipo desarrolla este tipo de moléculas para intentar corregir defectos genéticos en pacientes con esclerosis lateral amiotrófica.
Lluís Montoliu, investigador del Centro Nacional de Biotecnología, en Madrid, quien resalta otra ventaja de las proteínas Cas primitivas. El potencial para la edición genética del sistema CRISPR se descubrió en bacterias de la especie S. pyogenes. Estos microbios pueden ocasionar infecciones, por lo que muchas personas tienen anticuerpos que pueden provocar reacciones inmunitarias contra el CRISPR extraído de ellos. Las Cas primitivas, en cambio, son muy diferentes de cualquier versión actual, por lo que no las detecta el sistema inmune, una gran ventaja para evitar rechazo en futuras aplicaciones médicas.
Miguel Ángel Moreno Mateos, experto en edición genética del Centro Andaluz de Biología del Desarrollo, celebra el nuevo estudio. “Es particularmente fascinante la resurrección de proteínas Cas9 antiguas y el análisis de su actividad miles de millones de años después”, destaca. “Estas Cas9 resucitadas presentan nuevas posibilidades con un potencial considerable en biotecnología, aunque deben llevarse a cabo más estudios y análisis para que esto sea una realidad”.
¿ES POSIBLE REVERTIR EL ENVEJECIMIENTO?
Estos científicos consideran que los principales factores del envejecimiento no son mutaciones del ADN, sino errores en las instrucciones "epigenéticas", que provocan un desajuste.
Sus hallazgos arrojan luz sobre el proceso de envejecimiento ya que, hasta ahora se creía que el envejecimiento celular obedecía a las mutaciones del ADN - que alteran las células y, en última instancia, provocan la muerte celular -. Sin embargo, no todas las células de las personas mayores presentan mutaciones, ni tampoco los animales o las personas que tienen una mayor carga de células mutadas envejecen prematuramente.
Por ello, los científicos se centraron en otra parte del genoma, el "epigenoma". Los "epigenomas" son proteínas y sustancias químicas que se sitúan sobre cada gen para decirle qué tiene que hacer, dónde tiene que hacerlo y cuándo tiene que hacerlo. El "epigenoma" da instrucciones diferentes a cada célula sobre qué genes deben activarse y cuáles deben silenciarse.
Los científicos que han realizado esta investigación afirman que el envejecimiento se debe a la pérdida de instrucciones que la células necesitan para seguir funcionando. Las células pierden la capacidad de leer su ADN, de forma que "olvidan" cómo funcionar. Es lo que estos científicos denominan "Teoría de la Información del Envejecimiento".
Lo que estos estudiosos proponen es retrasar el "reloj" de la células adultas para que recuperen su identidad. En los experimentos que realizaron, estos científicos introdujeron roturas en el ADN de ratones jóvenes para envejecerlos y éstos empezaron a mostrar signos de vejez, como pelaje gris, menor actividad, mayor fragilidad, etc... A partir de ahí, revirtieron el proceso y lo que hicieron fue utilizar en las células renales y cutáneas los conocidos como "factores de Yamanaka", que son secuencias especificas del ADN que, al ser activadas externamente mediante proteínas asociadas, son capaces de rejuvenecer la célula.
UNA PROTEÍNA ARTIFICIAL DISEÑADA PARA DEGRADAR PLÁSTICOS
Un grupo de científicos españoles pertenecientes al Instituto de Catálisis y Petroleoquímica del CSIC, al Centro Nacional de Supercomputación de Barcelona y a la Universidad Complutense de Madrid han desarrollado proteínas artificiales que pueden degradar microplásticos de tereftalato de polietileno (PET), el cual es uno de los materiales más utilizados en envases y botellas. Al degradar este material se reduce a sus componentes esenciales, lo que permite su reciclaje o descomposición.
Para realizar esto han rediseñado una proteína de defensa (la fragacetoxina C) de la anémona de fresa (Actinica fragacea). La han modificado de forma que han construido una enzima hidrolítica que se ensambla en forma de nanoporos catalíticos sobre un modelo de membrana. Los tres aminoácidos que han diseñado se comportan como tijeras capaces
de descomponer el PET hasta pequeños fragmentos en condiciones
ambientales.
No solo es capaz de degradar el PET, sino también hay posibilidades de que se pudiesen degradar otros poliésteres presentes en ciertos bioplásticos. Todo esto ha sido realizado con inteligencia artificial y superordenadores.
 Este descubrimiento puede tener un gran impacto en nuestras vidas. El PET forma parte de más del 10% de la producción de plásticos a nivel mundial y su reciclaje es poco e ineficiente. El método que se ha estado utilizando hasta ahora era someter el plástico a altas temperaturas, lo que conlleva grandes emisiones de CO2.
Este descubrimiento puede tener un gran impacto en nuestras vidas. El PET forma parte de más del 10% de la producción de plásticos a nivel mundial y su reciclaje es poco e ineficiente. El método que se ha estado utilizando hasta ahora era someter el plástico a altas temperaturas, lo que conlleva grandes emisiones de CO2.
Con este nuevo método se proporciona una nueva alternativa viable en la que su degradación tiene entre un 5 y un 10 más de eficacia. Esta alternativa sería filtrar los nanoplásticos mediante membranas en la depuración de aguas residuales.
Optamos a un futuro mucho más limpio y sostenible en el que uno de los grandes problemas medioambientales como es el de las islas de plástico tendría una solución. Además, nuestras vidas que hasta ahora también peligraban debido al consumo de alimentos, como los peces, que llevan en su interior muchos de estos nanoplásticos estarían a salvo.
Fuentes: CSIC, National Geographic
EL COLESTEROL Y SU IMPORTANCIA PARA LA VIDA
martes, 28 de noviembre de 2023
UN EQUIPO CIENTÍFICO ESPAÑOL DESCUBRE UN PROCESO DE REGENERACIÓN DE TEJIDOS MUSCULARES

lunes, 27 de noviembre de 2023
REPARAN LOS TEJIDOS DE LOS PULMONES DAÑADOS POR TABACO
En la cita anual de la Sociedad Respiratoria Europea en Milán, el equipo de Wei Zou de la Facultad de Medicina de la Universidad de Tonji (Shangai) ha contado cómo esta terapia celular ha funcionado en un grupo de 17 pacientes que participaron en un ensayo clínico de fase I. Los resultados obtenidos se han reflejado en las actividades que han podido realizar meses después del tratamiento experimental: respiraban mejor, caminaban más y tuvieron una mejor calidad de vida después.
Se trata de una enfermedad respiratoria grave que consiste en un daño progresivo al tejido pulmonar. El tejido afectado no puede repararse con los tratamientos actuales, sólo aliviarse con medicamentos que ensanchan las vías respiratorias para mejorar el flujo de aire, conocidos como broncodilatadores.
El 80 % de los pacientes con EPOC han sido fumadores y uno de cada cuatro fumadores tiene la enfermedad. El tratamiento hasta el momento pasa, primero por el cese total del tabaco y, luego, una batería de opciones farmacológicas para aliviar la sintomatologías como los broncodilatadores o antibióticos en caso de infección, y en los casos más graves se llega a necesitar el trasplante de pulmón.
"Usamos un pequeño catéter que contiene un cepillo para recolectar las células progenitoras de las propias vías respiratorias de los pacientes. Clonamos las células para crear hasta mil millones más y luego las trasplantamos nuevamente a los pulmones de los pacientes mediante broncoscopia para reparar el tejido pulmonar dañado", explicó el responsable chino en rueda de prensa.
IMPRESIONANTES CÉLULAS SALVARON LA FLORA DE CHERNOBYL

Ya son 37 años del desastre nuclear que ocurrió Chernóbil en 1986, el cual causó cánceres en miles de personas de una zona muy poblada. Aunque también siguieron viviendo animales en la zona, los que mejor sobrevivieron fueron las plantas. De hecho, en las zonas más afectadas se recuperaron en tres años.
Si una dosis de radiación es alta, causa que las células se mueran rápidamente y el ADN se confunde y se daña. Estas dosis son letales en animales, pero en las plantas no, porque se desarrollan con el tiempo. Esto se debe a que las células vegetales pueden crear todo tipo de nuevas células que necesite la planta, por lo que es muy fácil reemplazar células o tejidos muertos.
La radiación también puede crear tumores, pero estos no se extienden a otras partes de la planta por las paredes rígidas que protegen la célula. También hay plantas que utilizan mecanismos varios para proteger el ADN, uno de ellos es cambiar su química para que sea más resistente y activar los sistemas para la reparación en caso de no funcionar lo primero.
Aun con todos estos sistemas de defensa, hay una parte de Chernóbil en la que la flora no aguantó la radiación al principio. Estoy hablando del Bosque rojo, el cual está cerca de la central y en donde la flora se volvió de color rojo y murió.EL VERDADERO ORIGEN DE LAS ESFERAS METÁLICAS
El heterodoxo astrónomo Abraham Loeb saltó a todos los medios de comunicación de todo el mundo en
2017, cuando lanzó la hipótesis de que el asteroide Oumuamua podría ser una nave extraterrestre.
El Departamento de Defensa de EE.UU. observó una brillante bola de fuego que sobrevoló el Océano Pacífico Sur, en las proximidades de Nueva Guinea. Estudiando su trayectoria y velocidad, el profesor Loeb y sus colaboradores concluyeron en 2019 (tras el episodio de Oumuamua), que esa bola de fuego también había llegado desde más allá del sistema solar, es decir, también tenía un origen interestelar y que cabía la posibilidad de que también fuese una nave extraterrestre. El meteorito fue bautizado como IM1 (Interstellar Meteorite -1).
En 2021, Loeb preparó un proyecto, denominado Galileo, encaminado a localizar objetos que pudieran ser procedentes de equipos tecnológicos extraterrestres. En junio de 2023, en el marco de este proyecto, organizó una expedición para rastrear los posibles restos de la bola de fuego IM1 que podrían haber quedado depositados en el fondo del Pacífico. El proyecto Galileo está financiado con más de con 1,5 millones de euros gracias a donaciones privadas de varias fundaciones y personas, entre ellas el magnate de las criptomonedas Charles Hoskinson.
 Como resultado de la expedición, Loeb anunció rápidamente que había localizado medio centenar de esférulas metálicas que solo podrían haber sido originadas en un exoplaneta (fuera del sistema solar) o ser los restos de una nave extraterrestre. Loeb presentaba así ideas similares a las que ya había avanzado para el debatido objeto Oumuamua. Los resultados fueron hechos públicos en una prepublicación.
Como resultado de la expedición, Loeb anunció rápidamente que había localizado medio centenar de esférulas metálicas que solo podrían haber sido originadas en un exoplaneta (fuera del sistema solar) o ser los restos de una nave extraterrestre. Loeb presentaba así ideas similares a las que ya había avanzado para el debatido objeto Oumuamua. Los resultados fueron hechos públicos en una prepublicación.
Las esférulas encontradas por Loeb tiene menos de un milímetro de tamaño. Antes de la expedición del proyecto Galileo, dragando otras zonas de los fondos oceánicos, ya se habían recogido muchas partículas de este estilo. Muchas de ellas habían sido reconocidas como de origen meteorítico y se habían calificado como "esférulas cósmicas": son pequeños fragmentos de meteoros que penetran en la atmósfera y que adquieren su peculiar forma esférica al quemarse por la fricción con los gases atmosféricos.
El medio científico siempre se mostró escéptico frente a las afirmaciones de Loeb: que la composición química de sus esférulas no fuese típica de meteoritos interplanetarios no garantizaba que su origen fuese interestelar y, mucho menos, que su origen fuese una nave espacial extraterrestre.
Fuente: El Mundo
domingo, 26 de noviembre de 2023
DESCUBREN LAS CÉLULAS QUE CAUSAN METÁSTASIS EN EL CÁNCER DE COLON
DESCUBREN UNA NUEVA PROTEÍNA EN MALAGA
El equipo aún continúa trabajando en este proyecto y buscan obtener una financiación para poder dar a conocer estos resultados y así el poder atraer la atención del mayor número de compañías farmacéuticas que puedan estar interesadas en colaborar en los ensayos requeridos para así poder llevar este prometedor medicamento al mercado.
sábado, 25 de noviembre de 2023
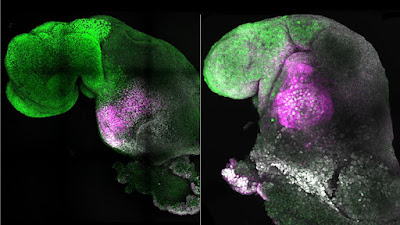
NUEVOS EMBRIONES SINTÉTICOS CON CORAZÓN Y CEREBRO
Este increíble hecho lo han llevado a cabo el equipo dirigido por la profesora Magdalena Zernicka-Goetz empleando este tipo de células que permiten crear todos lo tipos de tejidos del organismo, permitiendo haber ido progresando a través de las etapas de desarrollo del corazón y cerebro, así como de otros órganos vitales para el embrión como el saco vitelino que permite obtener los nutrientes necesarios. Sin embargo, en esta ocasión, se había obtenido un corazón que comenzaba a latir y un cerebro bastante desarrollado.
Por otra parte, aunque este ha sido un gran avance, la mayoría de estructuras se han desarrollado de forma incompleta o dañada.
 Pero después de diez años de experimentación, esto va a ser muy útil para conocer las razones por las que, en los humanos, algunos embarazos se desarrollan correctamente mientras que otros fracasan, ya que se sabe que en un embrión existen tres tipos de células madre que desarrollan el embrión enviando señales mecánicas y químicas entre ellas, permitiendo un buen desarrollo embrionario. Y si esto no ocurre lo más probable es que ocurran malformaciones, enfermedades...
Pero después de diez años de experimentación, esto va a ser muy útil para conocer las razones por las que, en los humanos, algunos embarazos se desarrollan correctamente mientras que otros fracasan, ya que se sabe que en un embrión existen tres tipos de células madre que desarrollan el embrión enviando señales mecánicas y químicas entre ellas, permitiendo un buen desarrollo embrionario. Y si esto no ocurre lo más probable es que ocurran malformaciones, enfermedades...
También se ha visto que este experimento serviría para reparar y desarrollar órganos humanos sintéticos que podrían ser usados en trasplantes. Así como para estudiar lo mecanismos del neurodesarrollo, ya que poco a poco se creará algún embrión en el que se haya conseguido generar un cerebro entero.
La profesora Magdalena comenta que este experimento supondrá un gran avance en la salud humana, pero realmente no se saben que efectos en el desarrollo puede tener en embriones humanos, pudiendo causar gran impacto social, por ello es importante considerar las consecuencias y aspectos morales y éticos del experimento.
Fuentes: El Periódico de España, El Diario
NUEVO TIPO DE CÉLULA DENTRO DE NUESTRO CEREBRO
célula cerebral. Este novedoso descubrimiento abre las puertas a un estudio más preciso de enfermedades como el alzheimer o el parkinson.
En nuestro cerebro, además de tener 86.000 millones de neuronas también podemos encontrar las células gliales. Ambas son fundamentales y trabajan conjuntamente para el buen funcionamiento de nuestro sistema nervioso, pero poseen características y funciones diferentes.
Entre las células gliales encontramos los astrocitos, que son células de forma estrellada que ofrecen soporte estructural a las neuronas, facilitan la transmisión de nutrientes y participan en la regulación de la concentración de iones y neurotransmisores en el espacio exterior. Los astrocitos están involucrados en procesos de información superior y el primer investigador en observarlo fue un español, Alfonso Araque, que actualmente se encuentra en la Universidad de Minnesota. En 1999, Araque abandonó el tópico del beso entre dos neuronas y propuso el concepto de "sinapsis tripartita".
Tras el estudio, Volterra y su equipo han descubierto un nuevo tipo de célula que la han descrito como híbrida. La han bautizado como "astrocitos glutamatérgicos". Es una subpoblación de astrocitos que comparte características con las neuronas por su capacidad de liberar glutamato. El equipo del neurocientífico italiano ha observado también que los astrocitos glutamatérgicos desempeñan un papel importante en un circuito que controla los movimientos y afecta al parkinson.
Volterra ya ha anunciado planes para investigar la distribución de esta célula en otras regiones cerebrales. Gracias a estas investigaciones podremos saber más sobre trastornos neuronales como el esquizofrenia o la esclerosis lateral amiotrófica.
Con estos estudios podemos comprobar que el cerebro es uno de los órganos más complejos de nuestro organismo.
Fuentes: National Geographic, El País
EL OXÍGENO DE LA TIERRA IRÁ REDUCIENDOSE
domingo, 12 de noviembre de 2023
SÍNDROME DEL INTESTINO PERMEABLE
“El tracto intestinal debe ser al menos un poco poroso y permeable. Debe permitir la absorción de agua y nutrientes de los alimentos digeridos, como el sodio, y de moléculas pequeñas, como la glucosa”, afirma Camilleri.
VIRUS DE LA GRIPE EN LA LECHE DE VACA PASTEURIZADA
Un equipo de científicos de la Universidad de Wisconsin-Madison ha descubierto por primera vez la presencia de virus de gripe aviar altament...

-
Un equipo de científicos de la Universidad de Wisconsin-Madison ha descubierto por primera vez la presencia de virus de gripe aviar altament...
-
Actualmente, los rinocerontes blancos ( Ceratotherium simum ) están en una situación extremadamente delicada, solo quedan 2 en Ol Pejeta Con...
-
La bacteria “Vibrio vulnificus” está siendo causa de preocupación sanitaria en Estados Unidos este verano. En los últimos meses se han conta...



































.jpg)